Auteurs: Dr. Amy de Haar-Holleman en Dr. Sofie Joris, medisch oncologen aan het UZ Brussel (VUB)
Wat is pancreaskanker?
De pancreas.
De pancreas, of alvleesklier, is een orgaan wat is gelegen in de bovenbuik. Het ligt achter de maag en mondt uit in de twaalfvingerige darm, dicht bij de galwegen. De pancreas maakt deel uit van het spijsverteringsstelsel en heeft 2 belangrijke functies. De eerste is de productie en afscheiding van sappen die betrokken zijn bij de vertering van voedsel en de opname van vetten, suikers en eiwitten. De tweede functie is de productie en afscheiding van hormonen, voornamelijk insuline en glucagon, die als taak hebben de bloedsuikerspiegel onder controle te houden.
Soorten pancreaskanker.
Pancreaskanker ontstaat als cellen van de pancreas ontsporen en ongelimiteerd gaan delen. Slechts 5% van de pancreastumoren ontstaan in de cellen die hormonen produceren. Verreweg de meeste pancreaskanker, namelijk 95%, ontstaan in de cellen die de spijsverteringsenzymen maken. Hiervan is de meest voorkomende, ruim 90% een adenocarcinoom, ook wel PDAC genoemd.

Figuur 1: de ligging van de pancreas
Symptomen bij pancreaskanker.
De symptomen die optreden bij pancreaskanker zijn te verklaren door de de ligging van de pancreas ten opzichte van andere organen. Als de tumor op de galwegen drukt, de groene verbinding tussen galblaas en dunne darm, zal er door verstoorde afvoer van het gal geelzucht optreden. Hierbij wordt de huid geen, de urine donker worden en kan de huid gaan jeuken. Als de hormoonproducerende cellen worden overwoekerd zal er suikerziekte of diabetes ontstaan. Als de cellen die spijsverteringssappen produceren overwoekerd worden, zal er vettige, lichte stoelgang en gewichtsverlies ontstaan. Door druk op zenuwen kan er buikpijn ontstaan, die meestal uitstraalt naar de rug. En tenslotte zien we vaak bij mensen met kanker in het algemeen en bij mensen met pancreaskanker in het bijzonder dat er klonters of stolsels in bloedvaten ontstaan, wat bijvoorbeeld kan leiden tot een trombosebeen.
Risicofactoren voor pancreaskanker.
Er zijn verschillende risicofactoren voor het ontstaan van pancreaskanker. Bij ongeveer 5-10% van de mensen met pancreaskanker is de oorzaak genetisch. Dat wil zeggen dat door ze door de aanwezigheid van een foutje in het erfelijk materiaal in de lichaamscellen een verhoogde kans hebben op het ontwikkelen van een tumor in de pancreas. Hierover zullen we in het volgende hoofdstuk meer vertellen. Daarnaast zijn er andere risicofactoren, waarvan roken de sterkste lijkt. De overige risicofactoren, zoals overgewicht, hoge leeftijd, het mannelijk geslacht, een chronische ontsteking van de pancreas, alcohol, een langer bestaande of juist een nieuwe diagnose suikerziekte en alcohol, geven allen ook een verhoogd risico op pancreaskanker, maar minder sterk dan roken.

Figuur 2: risicofactoren voor het krijgen van pancreaskanker
Hoe wordt de diagnose gesteld?
Als je klachten hebt die passen bij pancreaskanker zal de huisarts je naar het ziekenhuis verwijderen voor verder onderzoek. Tijdens de eerste consultatie zal meestal lichamelijk en een bloedonderzoek worden gedaan door de arts in het ziekenhuis. Bij het lichamelijk onderzoek kan de arts kijken of er een massa voelbaar is in de bovenbuik. In het bloedonderzoek kan de arts zien of de organen goed werken, of er bijvoorbeeld een probleem is met de afvoer van gal en of de tumormarker verhoogd is. Dat is een stofje dat sommige, maar niet allen pancreastumoren, produceren en aan het bloed afgeven. Als er aanhoudend verdenking is op pancreaskanker zal er aanvullend onderzoek worden gepland.
Er zijn verschillende onderzoeken die gedaan kunnen worden om de pancreas in beeld te brengen. Meestal wordt een endo-echografie (EUS) gedaan. Bij dat onderzoek wordt via de mond een flexibele slang met aan het einde een klein echoapparaat ingebracht om via de slokdarm, de maag en de dunne darm de organen die in de directe omgeving liggen, zoals de pancreas, de lever en galblaas, te bekijken. Als de tumor gezien wordt kan er direct wat weefsel weggenomen worden om onder de microscoop te bekijken, een biopsie. Daarnaast wordt een CT-scan van de borstkas en de buik gemaakt om te bekijken (1) wat de lokale situatie is en of de patiënt geopereerd kan worden en (2) of er uitzaaiingen op afstand zijn, bijvoorbeeld in de lever en de longen. Een MRI kan gebruikt worden om de pancreas gedetailleerder in kaart te brengen. Tenslotte worden alle bevindingen in een groep van bij de behandeling betrokken medisch specialisten besproken, het multidisciplinair oncologisch consult (MOC). In de MOC wordt het behandelplan gemaakt wat vervolgens met de patiënt besproken wordt. Voor de keuze van de behandeling houden artsen rekening met het stadium van de ziekte, de plaats en de grootte van de tumor, maar ook met de conditie, leeftijd en wensen van de patiënt.
De behandeling van pancreaskanker
De meest toegepaste behandelingen van pancreaskanker zijn een operatie (chirurgie) en een behandeling met medicijnen (chemotherapie). Soms wordt bestraling (radiotherapie) gebruikt, al dan niet in combinatie met chemotherapie. Een van de grootste problemen bij pancreaskanker is dat er pas laat in het ziektebeloop klachten optreden en de diagnose vaak pas in een laat stadium wordt gesteld. Hierdoor kan maar bij ongeveer 1 op de 5 patiënten kan de tumor met een operatie worden verwijderd. Soms kan dat direct, maar meestal moet de tumor eerst iets kleiner gemaakt worden door eerst chemotherapie te geven. Helaas wordt bij de overige 4 op de 5 patiënten de ziekte pas in een laat stadium gevonden en zijn er al uitzaaiingen of is de tumor te veel om de bloedvaten geen gegroeid. Bij deze mensen volgt een palliatieve behandeling, die bestaat meestal uit chemotherapie. Deze behandeling geneest de ziekte niet, maar kan de tumorgroei wel remmen en daarmee de klachten ten gevolge van de pancreastumor verminderen.
De overleving van pancreaskanker
Bij de diagnose wordt pancreaskanker in 4 stadia ingedeeld. Bij stadium I is er een kleine tumor en in de alvleesklier en zijn er geen uitzaaiingen. Patiënten met een stadium I pancreaskanker zijn de beste kandidaten voor een operatie. Bij stadium II is de tumor groter en kan het zijn dat er uitzaaiingen zijn naar een of meerdere lymfeklieren dicht bij de pancreas. Bij stadium III zijn behalve de tumor ook uitzaaiingen naar de lymfklieren en kan er zelfs al doorgroei zijn naar aanliggende bloedvaten. Bij stadium IV is de pancreaskanker verspreid naar organen die verder weg liggen van de pancreas, zoals de lever, longen of de buikholte. Hoe hoger het stadium bij diagnose, hoe slechter de overleving. In stadium I leven 42% ban de mensen nog 5 jaar na diagnose en bij stadium IV is dit slechts 42%.
Genetische mutaties bij pancreaskanker
Kanker ontstaat door gendefecten of mutaties in een cel, die meestal toevallig ontstaan. Slechts in uitzonderlijke gevallen is zo’n defect erfelijk. Elke dag ontstaan er gendefecten in cellen, maar doorgaans kan de cel deze schade zelf herstellen. Wanneer de schade te groot is, schakelt de cel zichzelf uit. Bij kanker verloopt dit proces anders: de cel verliest de controle, blijft zich ongecontroleerd delen en vormt een tumor. Deze tumor kan gezonde weefsels binnendringen en via uitzaaiingen andere organen aantasten.
Genetische veranderingen die ons risico op kanker verhogen, kunnen tijdens ons leven ontstaan of aangeboren (erfelijk) zijn. De tijdens ons leven verkregen of ‘verworven’ genmutaties zijn het gevolg van willekeurige fouten in de celdeling, of door blootstelling aan toxische stoffen die het DNA veranderen zoals tabaksrook. In een minderheid van de gevallen zijn genmutaties aangeboren. In dat laatste geval wordt de genetische fout doorgegeven van ouder op kind. Voor genen die aanleg geven tot het ontwikkelen van kanker gebeurt dit volgens een autosomaal dominant overervingspatroon wat wil zeggen dat er 50% kans is dat de kinderen het risico overerven.
Kanker komt vaak voor, waardoor de kans groot is dat meerdere personen binnen één familie ermee te maken krijgen. Hoewel kanker erfelijk kan zijn, is dat meestal niet het geval. Erfelijke aanleg speelt slechts bij 5 tot 10 procent van de mensen met kanker een bepalende rol.
Wat de erfelijke aanleg of predispositie voor pancreaskanker betreft zijn er verschillende genen gekend. Ze worden opgedeeld in twee grote groepen:
- Erfelijke tumorsyndromen met een >10% cumulatief lifetime risico op ductaal adenocarcinoom van de pancreas.
Hieronder vallen de patiënten die drager zijn van een pathogene (ziekteverwekkende) variant in CDKN2A (erfelijk melanoom), PRSS1 (erfelijke pancreatitis) en STK11 (Peutz-Jeghers). - Erfelijke tumorsyndromen met een onbekend of <10% lifetime risico op ductaal adenocarcinoom van de pancreas.
Hieronder vallen de patiënten die drager zijn van een pathogene variant in BRCA1, BRCA2, ATM, PALB2, MLH1, MSH2, MSH6 en TP53.
Het life-time risico op het ontwikkelen van pancreaskanker varieert afhankelijk van het gen waarin de pathogene variant of mutatie zich voordoet en wordt eveneens beïnvloed door de familiegeschiedenis. Het is belangrijk om te vermelden dat het hier gaat om de kans dat een nieuwe kanker ontstaat in de pancreas en het niet gaat om een herval van een andere kanker onder vorm van een uitzaaiing (metastase) in de pancreas.
Wat is het risico op pancreaskanker voor een drager van BRCA1/2 of gelijksoortige mutatie?
Wanneer patiënten een genetische test ondergaan voor het opsporen van het erfelijk borst en eierstokkanker syndroom (HBOC), worden de volgende genen: BRCA1, BRCA2, CHEK2, PALB2, ATM, MLH1, MSH6, MSH2, BARD1, BRIP1, RAD51C, RAD51D en TP53 geanalyseerd. Alleen diegene in bold weergegeven, verhogen licht de kans om pancreaskanker te ontwikkelen. De kans om ooit pancreaskanker te ontwikkelen, bedraagt 1,7% in de Belgische bevolking. Bij mutatiedragers wordt dit risico uitgedrukt in een relatief risico (RR). Het relatief risico is in dit geval een schatting van het aantal keren dat de kans om pancreaskanker te krijgen groter is in mutatiedragers in vergelijking met de algemene bevolking. Van de genen die behoren tot HBOC, zijn pathogene varianten in BRCA1, BRCA2 of PALB2 het meest voorkomend in families met pancreaskanker. De syndromen die het hoogste risico inhouden om pancreaskanker te ontwikkelen zijn Peutz-Jeghers syndroom en erfelijke pancreatitis.
In Tabel 1 hieronder zijn de risico’s per gen weergegeven.
Syndroom | Genen | Lifetime risico |
HBOC | BRCA1 BRCA2 | 2.3-3.0 RR 3.5-10 RR |
Fanconi anemie | PALB2 | 2.4 RR |
Ataxia telangiectasia | ATM | 6.5 RR |
Peutz-Jeghers | STK11 | 11-55%, 132 RR |
FAMMM | CDKN2A | 15-20%, 47.8 RR |
Lynch syndroom | MLH1, MSH2, MSH6, (PMS2) | 8.6 RR |
Erfelijke pancreatitis | PRSS1, SPINK1 | 30-70%, 69 RR |
HBOC = hereditary breast and ovarian cancer, FAMMM= familial atypical multiple mole/melanoma syndrome, RR = relatief risico verhoging tov algemene bevolking
Vroege opsporing/preventie van pancreaskanker
Late diagnose in pancreaskanker
De overlevingskans van pancreaskanker is om meerdere redenen zeer beperkt. De belangrijkste reden is dat de diagnose in de meerderheid van de gevallen pas laat gesteld wordt (Figuur 3). Hierdoor is er geen operatie, dus genezing, meer mogelijk. Er zijn meerdere oorzaak voor de late diagnose van pancreaskanker.
Ten eerste geeft pancreaskanker typisch pas laat in het ziekteproces klachten geeft. En die klachten, zoals pijn in de bovenbuik, zijn meestal niet heel specifiek voor pancreaskanker. Ten tweede zijn de risicofactoren niet goed bekend zijn. Iedereen weet dat de kans klein is dat je longkanker krijgt als je niet rookt, maar bij pancreaskanker is dat minder duidelijk. Ten derde zitten er beperkingen aan de huidige diagnostiek. Op een MRI of een endo-echografie kunnen afwijkingen, zeker als ze klein zijn, worden gemist. Tenslotte is er geen screeningsprogramma voor pancreaskanker in België, zoals er bijvoorbeeld wel voor borst- en darmkanker is. Of dat een groot gemis is, daar komen we verder in de tekst op terug. Al met al is de conclusie dat pancreaskanker door meerdere oorzaken meestal in een laat stadium wordt ontdekt en dat een belangrijke manier om de overleving te verbeteren vroege opsporing en preventie is.

Figuur 3: Stadium pancreaskanker bij diagnose
Definities: preventie, screening and surveillance
Het is belangrijk om goed te begrijpen wat de verschillende termen betekenen. Preventie wil in dit geval zeggen, levensstijlaanpassingen om het ontwikkelen van de ziekte te voorkomen. Bijvoorbeeld in geval van pancreaskanker: niet roken, geen alcohol gebruik en overgewicht vermijden. Screening is het implementeren van periodieke onderzoeken in de bevolking voor ziektes die zeer frequent voorkomen en waarmee men een diagnose in een vroeg stadium beoogt. In geval van kanker bestaat er een bevolkingsscreening voor borst, darm en baarmoederhalskanker. Surveillance (of controles) wil zeggen dat men periodieke onderzoeken inplant bij patiënten waarvan men weet dat ze drager zijn van een erfelijke aanleg die het risico op een bepaalde aandoening, in dit geval pancreaskanker verhoogt. Als men vroegtijdig de diagnose stelt, voordat de patiënt symptomen heeft, is het vaak goed behandelbaar.
De preventie van pancreaskanker
De bekende risicofactoren voor het krijgen van pancreaskanker zijn onder te verdelen in modificeerbare risicofactoren, dat wil zeggen risicofactoren die je zelf aan kunt passen en de niet-modificeerbare risicofactoren, waarbij dit niet het geval is. Voorbeelden van niet-modificeerbare risicofactoren zijn je erfelijke aanleg en je leeftijd, daar valt niet aan te veranderen. Door modificeerbare risicofactoren, die samen te vatten zijn als een ongezonde leefstijl, weg te nemen, kan je de kans op het ontwikkelen van pancreaskanker iets kleiner. Het neemt de kans op het ontstaan van kanker helaas niet weg.
Is screening zinvol?
Er is onderzoek gedaan of een screeningsprogramma voor pancreaskanker voor de hele bevolking, zoals bij borst- en darmkanker zinvol is. Dat bleek niet het geval te zijn. Doordat pancreaskanker niet heel vaak voorkomt, is het een programma wat wel veel veld kost, maar te weinig mensen zou identificeren. De onderzoeken toonden dus eerder schade (door overdiagnostiek en overbehandeling) aan dan voordeel voor de mensen die de screening ondergingen.
Screening in mensen met een verhoogd risico op het ontwikkelen van pancreaskanker, een hoog-risico populatie, bleek wel zinvol te zijn. Een hoog-risico populatie kenmerkt zich doordat de mensen een bepaalde genetische afwijking, dat wil zeggen fout in hun DNA, hebben die gepaard gaat met een verhoogde kans op het ontwikkelen van pancreaskanker (zie Tabel 1). Onderzoek in een hoog-risico populatie toonde aan dat de mensen die deelnamen aan een surveillance programma de kanker vaker in een vroeger stadium werd ontdekt, daardoor vaker voor chirurgie in aanmerking kwamen en een beter overleving hadden.
In de nationale en internationale richtlijnen dienen BRCA1/2 dragers (of dragers van een ander HBOC gen met een risico op pancreaskanker) enkel periodieke onderzoeken te verrichten om pancreaskanker vroegtijdig op te sporen als er familiale antecedenten van pancreaskanker zijn. Men start met deze onderzoeken vanaf 50 jaar of vanaf de leeftijd waarop het familielid de diagnose kreeg. Spreek steeds uw behandelend arts aan om te bekijken wat de beste strategie voor u is.
Onderzoek vroege opsporing/detectie pancreaskanker
Zoals al besproken is de late diagnose een zeer belangrijke oorzaak voor de slechte overleving van pancreaskanker. Hierdoor is het belangrijk onderzoek te doen naar vroege opsporing van pancreaskanker. Er wordt gelukkig op verschillende gebieden onderzoek verricht om de vroege opsporing verder te verbeteren.
Het opzetten van een goed surveillance programma begint eigenlijk bij de basis. Met het oog op enerzijds een zo minimaal mogelijke belasting van de deelnemers aan het programma en anderzijds een zo optimale opbrengt wil je bij voorkeur de surveillance het liefst aanbieden aan mensen die de grootste kans maken om daadwerkelijk pancreaskanker te ontwikkelen. Hiervoor is een betere inschatting van het risico op pancreaskanker nodig, maar ook betere diagnostische middelen.
Betere inschatting risico op pancreaskanker
Zoals gezegd zijn de leefstijl risicofactoren op het ontstaan van pancreaskanker onvoldoende sterk om dat als criterium te kunnen gebruiken voor deelname aan een surveillance programma. Door gestructureerde vragenlijsten aan mensen met pancreaskanker aan te bieden, kunnen er mogelijk nieuw risicofactoren worden gevonden. Meest waarschijnlijk wordt het risico op het ontstaan van pancreaskanker niet door een, maar juist het gelijktijdig bestaan van meerdere risicofactoren bepaald. Als de risicofactoren beter in kaart zijn gebracht, kan geprobeerd worden een model te maken, waaruit op basis van aan- en afwezigheid van risicofactoren een laag, hoog of middelmatig risico op het ontwikkelen van pancreaskanker komt.
Naast risicofactoren qua leefstijl zijn er ook erfelijke risicofactoren. Door het DNA van grote groepen patiënten met pancreaskanker te bekijken, kunnen er naast de bekende fouten in het genetisch materiaal ook een patroon gevonden worden van kleine veranderingen in het DNA die bij meerdere patiënten voorkomen. Net als bij de leefstijl risicofactoren kunnen de erfelijke risicofactoren ook in een model verwerkt worden, waaruit op basis van aan- en afwezigheid van risicofactoren een laag, hoog of middelmatig risico op het ontwikkelen van pancreaskanker komt. Zo’n model heet een polygene risico score.
Naar verwachting geeft een risico score gebaseerd op de aan- en afwezigheid van leefstijl en genetische factoren de beste voorspelling. Om deze risicomodellen zo nauwkeurig mogelijk te maken is echter een hele grote inspanning nodig met data van duizenden patiënten.
Betere diagnostiek pancreaskanker: biomarkers
Een biomarker is een meetbare stof in het lichaam die iets zegt over de aanwezigheid van een ziekte. In onze context over de aanwezigheid van pancreaskanker. Biomarkers kunnen in alle lichaamsvloeistoffen gemeten worden, maar worden in de praktijk vaak in het bloed gemeten. Momenteel wordt er bij een bloedafname bij iemand met de verdenking pancreaskanker onder ander de tumormarker Ca19.9 bepaald. Een ideale tumormarker wordt alleen door de tumor en niet of nauwelijks door normale lichaamscellen gemaakt. Ca19.9 is geen ideale tumormarker, omdat het ten eerste niet door alle pancreaskankers geproduceerd wordt en ten tweede ook geproduceerd wordt als reactie op andere oorzaken, bijvoorbeeld problemen met de galwegen.
Ca19.9 is voorbeeld van een eiwit wat een pancreastumor kan produceren. De zoektocht naar een goede tumormarker gaat verder dan alleen op eiwitniveau. Er zijn ook andere sporen van een tumor terug te vinden in lichaamsvloeistoffen zoals bloed, urine en speeksel. In het bloed kunnen ook circulerende tumorcellen worden aangetroffen die los hebben gelaten van de tumor of zelfs het erfelijk materiaal van de tumor (DNA, RNA of microRNA). Ook stofwisselingsproducten van de tumor (metabolieten). Deze producten kunnen los in de lichaamsvloeistoffen aangetroffen worden, maar bevinden zich soms ook in vetblaasjes (exosomen). Ook kunnen afweercellen een afweerreactie tegen de tumor maken, waardoor er tumorspecifieke antilichamen worden aangetroffen.
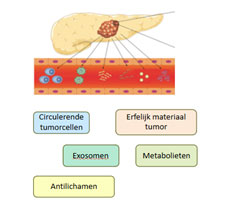
Figuur 4: Voorbeelden van diagnostische biomarkers bij pancreaskanker
Internationale samenwerking
Om tot nieuwe diagnostische biomarkers en risicofactoren te komen bij een ziekte die zo relatief zeldzaam is als pancreaskanker is het nodig om internationaal de krachten te bundelen. Er zijn verschillende initiatieven opgericht met dit doel.
PRECEDE is een consortium waaraan ziekenhuizen in zowel de Verenigde Staten als Europa deelnemen. Binnen PRECEDE wordt aan mensen met een hoog risico op het ontwikkelen van pancreaskanker een surveillance programma aangeboden. De deelnemende ziekenhuizen nemen vragenlijsten en bloed-, urine- en speekselstalen af bij patiënten die deelnemen aan het programma en sturen die op naar een centraal punt in Amerika. Hier worden de stalen opgeslagen en later geanalyseerd. De antwoorden op de vragenlijsten worden in een grote onderzoeksdatabase ingevoerd. Krachtige computers hiermee aan de slag om te proberen met behulp van deze gegevens risicomodellen te maken. Het UZ Brussel is in bezig onderdeel te worden van PRECEDE, maar door andere wetgeving in Amerika en Europa is dat een uitdagend proces. Het CAPS-consortium is een voorbeeld van een soortgelijk, wat kleiner, initiatief.



 BRCA+ Network asbl
BRCA+ Network asbl